Índice:
- Peligros
asociados con especies de garrapatas
- Distribución
geográfica
- Entomología
- Biología
- Epidemiología
y transmisión de patógenos
- Salud
pública (vigilancia y control)
- Las áreas
actuales de incertidumbre
- Referencias
 |
| Hyalomma marginatum |
PELIGROS ASOCIADOS CON LAS ESPECIES DE GARRAPATAS
Antes de
2005 la proporción de Hyalomma marginatum entre las garrapatas recolectadas a
partir de estudios anteriores en Turquía no superar el 5%. Sin embargo en 2005,
el 74% de los bovinos estaban infestados de garrapatas, y el 85% de las
garrapatas recolectadas fueron Hyalomma marginatum [1].
Importación a través de las aves migratorias
Hyalomma
margintum es un ectoparásito común de aves paseriformes. Las larvas o
individuos inmaduros permanecen unidas al huésped (en este caso un ave) hasta
26 días, lo que permite su transporte pasivo a través de continentes [2-4].
Aunque es probable que las garrapatas en migrantes de larga distancia no pueden
sobrevivir, aves infestadas que migran distancias cortas tienen una mejor
oportunidad de establecer nuevas poblaciones locales.
 |
| carricerín común (Acrocephalus schoenobaenus) |
 |
| carricerín común (Acrocephalus schoenobaenus) |
 |
| carricerín común (Acrocephalus schoenobaenus) |
Importación a través de la ganadería
El ganado
es un riesgo particularmente alto de importar Hyalomma marginatum ya que pueden
soportar grandes infestaciones. No es raro para un máximo de 100 garrapatas Hyalomma
se encuentran en un animal [5]. El control de garrapatas en el ganado importado
es rara vez, o nunca, realizado.
Plasticidad ecológica
Garrapatas
Hyalomma marginatum tienen una gran capacidad para soportar una amplia gama de
temperatura y humedad [6]. La capacidad de la garrapata para adaptarse a una
amplia gama de condiciones y una variedad de hábitats, incluyendo desierto
árido, pantanos y matorrales hacen que sea extremadamente difícil de erradicarlas
a gran escala [7].
El riesgo de enfermedad
Hyalomma
marginatum es el principal vector del virus de la fiebre hemorrágica de Crimea-Congo
en Europa [8].
DISTRIBUCIÓN GEOGRÁFICA
África y Asia:
Hyalomma
marginatum está ampliamente distribuida en todo el norte de África y Asia,
donde se informa de Argelia, Armenia, Azerbaiyán, Egipto, Etiopía, Georgia,
Irán, Irak, Israel, Marruecos, Sudán, Siria, Túnez y Turquía [3,7,9].
Europa:
Hyalomma
marginatum está presente en Europa meridional y oriental, después de haber sido
grabado en Albania, Bosnia y Herzegovina, Bulgaria, Croacia, Chipre, Francia,
Grecia, Italia, Kosovo, la ex República Yugoslava de Macedonia, Moldavia,
Montenegro, Portugal, Rumania , Rusia, Serbia, España y Ucrania [3,7,9-11].
Varios
registros esporádicos también se han reportado para los animales importados,
humanos y aves migratorias en Alemania [12], Hungría [13], Rusia [14],
Finlandia [9], Países Bajos [15] y el Reino Unido [4,16], pero estos no
representan poblaciones establecidas.
Potencial para la futura propagación
Los
ectoparásitos como garrapatas tienen relativamente poca movilidad por sí
mismos, incluso Hyalomma marginatum. Sin embargo, pueden ser transportados a
grandes distancias por sus huéspedes vertebrados, en particular las aves
migratorias y ungulados. Una vez unido a la piel de un huésped se pueden
alimentar por un período de hasta treinta días. Es la duración de la fijación
que mejora su capacidad para la dispersión. Ganadería en particular, son un
riesgo particularmente alto de importar las garrapatas ya que pueden soportar
grandes infestaciones y no es raro que un máximo de 100 garrapatas Hyalomma marginatum se encuentren en un
animal [5]. Un estudio de las garrapatas que infestan las aves migratorias que
entran en el Reino Unido encontró que el 21% de las garrapatas recolectadas
fueron Hyalomma marginatum [4]. Las especies de aves más comúnmente infestados
con Hyalomma marginatum eran collalba gris (Oenanthe Oenanthe) y (Sylvia
communis), con cada ave positiva albergar 2-5 ninfas. Ninfas de Hyalomma marginatum también se encontraron
solas en carricerín común (Acrocephalus schoenobaenus) y colirrojo real
(Phoenicurus phoenicurus).
La
degradación de las tierras agrícolas que conduce a la invasión de matorral se
ha identificado como un factor de riesgo de explosiones de población de
Hyalomma marginatum, en particular cuando la tierra era previamente utilizada
para el pastoreo de ganado [3].
Las
poblaciones de la cuenca mediterránea (sur de Europa y norte de África) se
consideran en la actualidad que se rige por las precipitaciones y
evapotranspiración en verano. Una disminución en ambos sería probable que tenga
un impacto en el hábitat disponible para la garrapata y facilitar su
propagación hacia latitudes más septentrionales. Por el contrario, las poblaciones
de Europa oriental y el Cáucaso están regulados por las temperaturas mínimas a
finales de otoño. Las bajas temperaturas en ninfas de fuerza a finales de otoño
para pasar el invierno llena de sangre, con una alta tasa de mortalidad
posterior. Sin embargo, en regiones donde actualmente sobreviven, otoños más
cálidos están permitiendo para la muda de ninfas a los adultos, la disminución
de la mortalidad de la población y que permite la propagación gradual en
territorios vecinos adecuados [9]. Modelos de la distribución de Hyalomma
marginatum bajo escenarios de calentamiento del clima predicen que estas
garrapatas se apoyarían en algunos sitios donde aún no tienen presencia, aunque
algunas áreas en las que la garrapata es ahora presentes se convertiría hábitat
inadecuado en las mismas situaciones [35]. Las regiones que mostraron la mayor
probabilidad de colonización fueron Italia, al sur de los Alpes, los Balcanes,
Rumania, Ucrania, Moldavia, amplias zonas del sur de Rusia y algunas áreas de
Alemania y los Países Bajos [35].
Ganadería
de los Balcanes han sido previamente destacado como un factor de riesgo para la
importación Hyalomma marginatum en Europa occidental [9].
ENTOMOLOGÍA
NOMBRE DE
LAS ESPECIES / CLASIFICACIÓN: Hyalomma marginado Koch, 1844
Bajo el
género Hyalomma Koch, 1844, Hyalomma (Euhyalomma) marginatum Koch 1844 se
consideraban hasta entonces un grupo complejo de cuatro subespecies: Hyalomma
(E.) marginatum marginatum Koch, 1844; Hyalomma (E.) marginatum Rufipes Koch
1844; Hyalomma (E.) marginatum turanicum Pomerantzev, 1946 y Hyalomma (E.)
marginatum isaaci Sharif, 1928 [17].
En 2008,
Apanaskevich y Horak reevaluaron esta clasificación taxonómica que conduce al
restablecimiento de Hyalomma rufipes, Hyalomma
turanicum y Hyalomma isaaci como especies completas y Hyalomma marginatum ya no
se refiere como Hyalomma marginadtum.
 |
| Hyalomma rufipes |
SINÓNIMOS
COMUNES: Hyalomma mediterranea
OTROS
NOMBRES EN USO: Hyalomma plumbeum Panzer, 1795 (utilizado principalmente en los
países ex soviéticos) [3,18].
 |
| Hyalomma plumbeum |
 |
| Hyalomma plumbeum |
Claves de
identificación sugerida: Un reciente taxonómica re-evaluación integral del grupo de garrapatas Hyalomma 'marginatum' fue
publicado por Apanaskevich y Horak [3,18]. Información de utilidad también se
puede encontrar en [10,19-21]
Características
morfológicas / especies similares
Rufipes
Hyalomma (distinguibles por puntuaciones densos, densa setas circumspiracular y
forma de la placa espiracular); Hyalomma turanicum (distinguibles por
puntuaciones moderadamente densas, setas circumspiracular y forma de la placa
espiracular).
BIOLOGÍA
Ciclo vital
Hyalomma
marginatum es una garrapata ditropic, lo que significa que las larvas
congestionan permanecen en el mismo host a mudar y alimentar de nuevo como
ninfas. Los adultos buscan y se alimentan de una segunda persona de acogida
tras un período de diapausa [21]. Todas las etapas son generalmente más activo
en los meses de verano [3,22].
 |
| Hyalomma marginatum |
 |
| Hyalomma marginatum |
Ninfas
Activo
entre junio y octubre, con números de pico en julio y agosto [23,24]. Después
de la alimentación, los inmaduros ya sea i) separar a principios de verano, la
muda a los adultos durante la misma temporada y pasar el invierno como un
adulto o ii) las que alimentan a finales del verano Suelte con en septiembre /
octubre y pasan el invierno como ninfas, la muda a los adultos en la primavera
siguiente . Sin embargo, el primero es más común.
Adultos
Las
garrapatas adultas se activan en la primavera, cuando las temperaturas medias mensuales
llegan a 10,5 ° C. Ellas buscan activamente / esperan una acogida, cuando las
temperaturas medias diarias son 22 a 27 ° C y la humedad es del 75-100%. Cuando
aumenta la temperatura del aire por encima de 30 ° C y la temperatura del suelo
por encima de 45 ° C, las garrapatas prefieren esconderse o incluso enterrarse
en el suelo [23,25]. Los machos y las hembras se aparean en el huésped, pudiendo
un macho aparearse con muchas hembras durante varias semanas. Las hembras inseminadas
tras una ingesta caen fuera del huésped, ponen hasta 7 000 huevos en el suelo y
mueren. Las larvas eclosionan después de 20 a 40 días [22,26].
 |
| Hembra de Hyalomma marginatum |
Voltinismo
Por lo
general, hay un máximo de una generación por año [3,19,22].
Preferencia de huésped. Búsqueda de huésped
En contraste
con las garrapatas Ixodes spp. que espera pasivamente que pase un huésped en un
lugar elevado en la vegetación, las garrapatas Hyalomma sp. busca activamente a
sus huéspedes [3,23,27].
Adultos
Los adultos
de garrapatas Hyalomma prefieren alimentarse de animales grandes (Artyodactyla
y Perisodáctilos). Las garrapatas Hyalomma adultas se ocultan en el suelo y van
activamente hacia un huésped animal, cuando detectan ciertas señales,
incluyendo vibración, objetos visuales, dióxido de carbono, amoníaco o calor de
la temperatura del cuerpo del huésped. Pueden reconocer visualmente al huésped de
3-4 metros hasta 9 metros [7,27]. Los adultos de Hyalomma asiaticum pueden
seguir el huésped durante diez minutos o más y durante ese tiempo caminan /
correr una distancia de hasta 100 metros [27,28]. Observaciones similares
también se han registrado para Hyalomma marginatum (Vatansever, comunicación
personal).
Larvas
Los estados
inmaduros se alimentan preferentemente de pequeños mamíferos como Lagomorpha
(Lepóridos) y Insectivora (Erinaceidae) y aves terrestres forraje,
especialmente en los órdenes Passeriformes (Alaudidae y Corvidae) y Galliformes
(Phasianidae) [23,24,29] No les gusta que se alimentan de roedores [22,26]. Los
inmaduros se alimentan durante dos a tres semanas con un periodo de descanso de
tres semanas para varios meses si pasan el invierno [3,19].
 |
| Oenanthe Oenanthe |
 |
| Oenanthe Oenanthe |
 |
| Oenanthe Oenanthe |
Donde se colocan para alimentarse
En las aves
y pequeños y medianos mamíferos silvestres las garrapatas Hyalomma marginatum se
sitúan alrededor de la cabeza, sobre todo en y alrededor de las orejas [3]. En
liebres, las larvas se conectan primero a los márgenes de las orejas y después
de la muda las ninfas migran hacia la cara, el cuello y alrededor de los ojos
(Z Vatansever, comunicación personal). Además de unir a los seres humanos, los
adultos son especialmente comunes en el ganado y otros ungulados, incluyendo
caballos, ovejas, cabras, camellos, ciervos y jabalíes alimentación durante una
o dos semanas y el apareamiento en el huésped. En rumiantes las garrapatas Hyalomma
marginatum se congregan alrededor
de los cuartos traseros, en particular, la ubre, el escroto, el área inguinal y
el perineo [30].
Habitat
Garrapatas
marginatum Hyalomma prefieren el clima mediterráneo del norte de África y el
sur de Europa, con niveles bajos a moderados de humedad y una larga estación
seca durante los meses de verano. Ambos estados inmaduros y adultos se
encuentran característicamente en las estepas, sabanas y matorrales de las
colinas y los valles biotipos [3,9,10,19]. Ellos están ausentes en bosques de
hoja caduca Europea y bosque mixto biotipos contemporáneos y anteriores, cuando
se sustituyan principalmente por Ixodes ricinus y Dermacentor marginatus [3].
Umbrales / restricciones / criterios de desarrollo Ambientales
Umbrales ambientales / climáticos
Los adultos
son activos a temperaturas de más de 12 ° C [31,32] y larvas entre 14-16 ° C.
Poblaciones establecidas actualmente sólo mantienen cuando la acumulación anual
de temperaturas está entre 3.000 a 4.000 ° C y el déficit de vapor de agua está
por debajo de un promedio de 15 hPa [32].
Endurecimiento de la cutícula: larva-ninfa cinco días, ninfa-adulto
eigh8 días [23,32,33]. Alimentar período: Larva / ninfa 26 días, adultos 14
días [32].
Invernal
Las ninfas y adultos que se han alimentado son capaces de pasar el invierno sin alimentar, sin embargo las tasas de mortalidad se incrementan para tales ninfas en comparación con los adultos sin alimentar [22-24,26]. Las poblaciones han logrado sobrevivir a temperaturas de hasta -20 ° C en Rusia. Por debajo de esta temperatura, se han producido caídas drásticas de población [3].
Rango de
dispersión
Garrapatas
Hyalomma tienen ojos que son el principal receptor para encontrar huéspedes y
escondites bien desarrollado. En contraste con otras garrapatas tales como
Ixodes spp., Pueden migrar largas distancias horizontalmente. Por ejemplo,
Hyalomma asiaticum puede migrar hasta 500 metros en un mes, pero por lo general
se dispersan en un radio de 80-100m [34].
EPIDEMIOLOGÍA
Y la transmisión de patógenos
Vector de estado
Hyalomma
marginatum es considerado como el vector más importante del virus de la fiebre
hemorrágica de Crimea-Congo en Eurasia [3,8]. Aeschlimannii Rickettsia se ha
aislado de garrapatas Hyalomma marginatum importadas en Alemania, Hungría y
Rusia sobre aves migratorias [13,14,36]. Esta bacteria también se ha detectado
en Hyalomma marginatum recogido en Chipre [37], y en la isla italiana de
Pianosa, un sitio de parada importante para las aves migratorias [38]. Virus
Dhori [39], virus Bahig [40] y el virus de Matruh [41] también han sido aislados
de esta especie de garrapatas; sin embargo, su capacidad vectorial está aún por
determinar.
El virus de la fiebre hemorrágica de Crimea-Congo
Vector y
reservorio principal. El virus de la fiebre hemorrágica de Crimea-Congo se mantiene en la población de garrapatas
por transmisión trans stadial y trans-ovárica con el co-alimentación y
transmisión venérea demostrado por otra Hyalomma spp. [42].
 |
| Virus que ocasiona la fiebre hemorrágica de Crimea-Congo |
Características clínicas
La
infección en los animales, distintos de los ratones lactantes, es asintomática,
mientras que en los seres humanos CCHFV es capaz de inducir un síndrome
multisistémico grave asociada con fiebre, shock y hemorragia [43]. Por lo
general, el curso clínico sigue a cuatro fases distintas: la incubación,
pre-hemorrágicas, hemorrágicas y convalecencia.
El riesgo de enfermedad confirmada
El virus de
la fiebre hemorrágica de Crimea-Congo
es considerado como un patógeno emergente en Europa y la distribución de las
especies de vectores de garrapatas conocido actualmente es muy superior a la
del virus. La estacionalidad de los casos humanos se corresponde con el
principal período de actividad de las garrapatas (primavera y verano). El
riesgo de las aves migratorias importadores CCHFV través de las garrapatas se
prevé que sea muy baja [44]. En la última década el virus de la fiebre
hemorrágica de Crimea-Congo ha sido reconocido como un problema creciente en
Eurasia, que afecta a varios países del este de Europa (Albania, Bulgaria,
Kosovo y Rusia), incluida la aparición de casos clínicos en humanos en Turquía
(2002), Grecia (2008), Georgia (2009) y más recientemente en 2010, la India.
Los estudios de seroprevalencia también han encontrado evidencia de circulación
del virus en Hungría [45], Portugal [46] y, más recientemente Rumania [47]. El virus
de la fiebre hemorrágica de Crimea-Congo se ha detectado directamente en Hyalomma
marginatum recogido en Turquía [48-50], Bulgaria [51] y España [52].
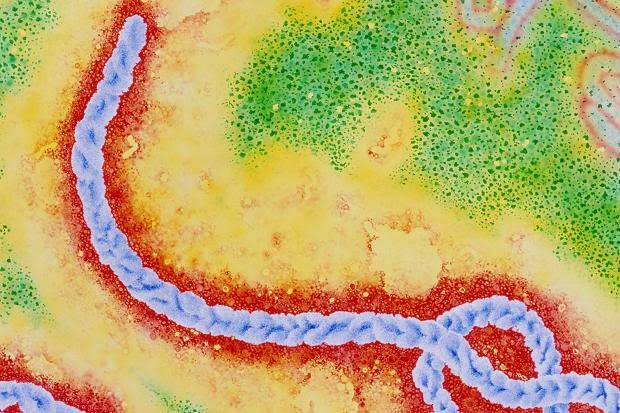 |
| Virus que ocasiona la fiebre hemorrágica de Crimea-Congo |
SALUD PÚBLICA (vigilancia y control)
Técnicas de recolección
Técnicas tradicionales
para muchas otras ixódidos son menos eficaces contra las garrapatas cazadores
como Hyalomma marginatum. En cambio, las garrapatas se pueden recoger
directamente en cantidad durante la alimentación o mientras buscan un huésped
(obtenida de la planta).
Métodos de control
Para
reducir el contacto con las poblaciones humanas áreas donde las garrapatas
pueden sobrevivir y de descanso de compensación (es decir, pajares, montones de
maleza, basura de hojas, etc.) tiene algunos beneficios [9]. Sin embargo, las
garrapatas Hyalomma marginatum están particularmente extendidas en las tierras
abiertas, campos de cultivo y matorrales, lo que hace el uso de acaricidas de acción
amplia son inviables. Parece que la forma más efectiva para controlar las
poblaciones Hyalomma marginatum
es el uso periódico de acaricidas en los rumiantes.
Los
principales grupos de acaricidas utilizados para el control de garrapatas
(dirigidos principalmente a la ganadería o alojamientos para el ganado) son:
los piretroides, ureas benzol-fenilo, lactonas macrocíclicas, spinosad y
fipronil [9]. Opciones para su uso incluyen tanques de inmersión, aerosoles o
pulverizadores de mano, utilizar complementos, SPOT-ons y fórmulas de engrase
para la aplicación específica [7].
Los seres
humanos pueden tomar medidas para evitar garrapatas en general, incluyendo el uso
de ropa protectora y usar repelente químico contra garrapatas como permetrina o
deltametrina. Se debe tener en cuenta que las preparaciones que son eficaces
contra otras garrapatas (Ixodes) son menos eficaces contra garrapatas Hyalomma. A veces pueden estimular la
respuesta adjunto en garrapatas
Hyalomma [53], [54].
ÁREAS DE CORRIENTE DE INCERTIDUMBRE
Hay poca
investigación sobre el nivel de resistencia de las poblaciones Hyalomma
marginatum, utilizando regularmente
acaricidas.
Hay algunas
pruebas que sugieren que las subpoblaciones de esta especie de garrapata se han
adaptado a nichos climáticos individuales [9] - se requiere más investigación
para explorar, si estas variaciones afectarán su propagación futura.
La razón o
combinación de razones que llevó a un gran aumento de la población en Turquía a
finales de 1990 / principios de 2000 todavía se están debatiendo. Sabemos que
en los lugares donde se produce la fiebre hemorrágica de Crimea-Congo hay un
aumento de la población marginado Hyalomma y por lo tanto el contacto
humano-garrapata. Sin embargo, las razones de este aumento son aún desconocidos
y en la actualidad sólo podemos especular. Estos escenarios incluyen:
1. Aumento
de la población de animales salvajes: observaciones personales, apoya la idea
de que las poblaciones de jabalí, liebre y otros animales silvestres han
aumentado en áreas la fiebre hemorrágica de Crimea-Congo. Desequilibrio ciclo depredador-presa local también ha sido
sugerido como elevar el riesgo de transmisión [55].
 |
| liebre |
2. La
práctica agrícola y la migración: Centrado en las zonas donde la agricultura
todavía se practica con herramientas primitivas y en su mayoría basada en los
esfuerzos humanos (por ejemplo, cuando toda la familia se dedica a la cosecha).
Del mismo modo, en los lugares donde se ha producido una migración hacia los
principales centros urbanos, dejando tierras abandonadas adecuadas para la vida
silvestre y la formación de matorral. Esto también puede verse afectada por los
cambios en el uso del suelo como resultado de cambios en los niveles de
importación de cultivos, reduciendo así la necesidad de cultivos locales, con
la tierra, posteriormente, volver las garrapatas a adecuado pastizales [55].
3. Cambios
en la cría de animales y medio ambiente: En Turquía, la población ovina en la
zona ha disminuido en un 60 a 70% desde 1990. El Ministerio de Medio Ambiente turco
ahora prohibe estrictamente el pastoreo de ovejas y cabras en monte y bosques.
a. Disminución de la población ovina
puede influir en el aumento de la liebre y una mayor población de aves [56,57]
[57].
b. Disminución de la población ovina
puede haber dado lugar a cambios en la composición de garrapatas (por ejemplo,
cambio de Rhipicephalus a Hyalomma)
 |
| Hyalomma marginatum |
REFERENCIAS Y BIBLIOGRAFÍA
1.
Vatansever Z, Uzun R, Estrada-Peña A, Ergonul O. Crimean-Congo haemorrhagic
fever in Turkey. In: Ergonul O, Whitehouse CA, editors. Crimean-Congo
hemorrhagic fever: A global perspective Dordrecht: Springer; 2007.
2. Kaiser MN, Hoogstraal H, Watson GE. Ticks (Ixodoidea) on migrating
birds in Cyprus, fall 1967 and spring 1968, and epidemiological considerations.
Bull Entomol Res. 1974; 64:97-110.
3. Hoogstraal H. The epidemiology of tick-borne Crimean-Congo
hemorrhagic fever in Asia, Europe, and Africa. J Med Entomol. 1979 May
22;15(4):307-417.
4. Jameson LJ, Morgan PJ, Medlock JM, Watola G, Vaux AG. Importation of
Hyalomma marginatum, vector of Crimean-Congo haemorrhagic fever virus, into the
United Kingdom by migratory birds. Ticks Tick Borne Dis. 2012 Apr;3(2):95-9.
5. Estrada-Pena A, Jameson L, Medlock J, Vatansever Z, Tishkova F.
Unraveling the ecological complexities of tick-associated Crimean-Congo
hemorrhagic fever virus transmission: a gap analysis for the western
Palearctic. Vector Borne Zoonotic Dis. 2012 Sep;12(9):743-52.
6. Bouattour A, Darghouth MA, Daoud A. Distribution and ecology of ticks
(Acari: Ixodidae) infesting livestock in Tunisia: an overview of eighth years
field collections. Parassitologia. 1999 Sep;41 Suppl 1:5-10.
7. Latif AA, Walker AR. An introduction to the biology and control of
ticks in Africa. International Consortium on ticks and tick borne diseases,
2004.
8. Ergonul O, Whitehouse CA. Crimean-Congo hemorrhagic fever: A global
perspective. Dordrecht: Springer; 2007.
9. EFSA. Scientific opinion on the role of tick vectors in the
epidemiology of Crimean-Congo hemorrhagic fever and African swine fever in
Eurasia. EFSA J. 2010;8(8):1703.
10. Estrada-Peña A, Bouattour A, Camicas JL, Walker AR. Ticks of
domestic animals in the Mediterranean region. A guide to the Identification of
species. . International Consortium on ticks and tick borne diseases (ICTTD-2).
INCO-DEV Programme, European Union, 2004.
11. ECDC. Vector distribution maps Stockholm: European Centre for
Disease Prevention and Control; 2013. Available from: http://www.ecdc.europa.eu/en/healthtopics/vectors/vector-maps/Pages/VBORNET-maps-tick-species.aspx.
12. Kampen H, Poltz W, Hartelt K, Wolfel R, Faulde M. Detection of a
questing Hyalomma marginatum marginatum adult female (Acari, Ixodidae) in
southern Germany. Exp Appl
Acarol. 2007;43(3):227-31.
13. Hornok
S, Csorgo T, de la Fuente J, Gyuranecz M, Privigyei C, Meli ML, et al. Synanthropic
birds associated with high prevalence of tick-borne rickettsiae and with the
first detection of Rickettsia aeschlimannii in Hungary. Vector Borne Zoonotic
Dis. 2013 Feb;13(2):77-83.
14. Movila A, Alekseev AN, Dubinina HV, Toderas I. Detection of
tick-borne pathogens in ticks from migratory birds in the Baltic region of
Russia. Med Vet Entomol. 2013 Mar;27(1):113-7.
15. ICTTD. Newsletter on ticks and tick-borne diseases of livestock in
the tropics, October. No. 37: ICTTD; 2008.
16. Jameson LJ, Medlock JM. Tick surveillance in Great Britain. Vector Borne
Zoonotic Dis. 2011 Apr;11(4):403-12.
17. Horak
IG, Camicas JL, Keirans JE. The Argasidae, Ixodidae and Nuttalliellidae (Acari:
Ixodida): a world list of valid tick names. Exp Appl Acarol.
2002;28(1-4):27-54.
18. Apanaskevich DA, Horak IG. The genus Hyalomma Koch, 1844: V.
re-evaluation of the taxonomic rank of taxa comprising the H. (Euhyalomma)
marginatum Koch complex of species (Acari : Ixodidae) with redescription of all
parasitic stages and notes on biology. Int J Acarol. 2008 Mar;34(1):13-42.
19. Pomerantzev BI. Ixodid ticks (Ixodidae). . In: Anastos G, editor.
Fauna of USSR volume IV, no 2. Washington: The American Institute of Biological
Sciences; 1959.
20. Feldman-Muhsam B. Revision of the genus Hyalomma. I. Description of
Koch's types. . Bull Res Council Israel. 1954;4:150-70.
21. Walker A, Bouattour A, Camicas JL, Estrada-Pena A, Horak IG, Latif
AA. Ticks of domestic animals in Africa. A guide to the identification of
species. International Consortium on ticks and tick borne diseases (ICTTD-2).
INCO-DEV Programme, European Union, 2003.
22. Kotti BK, Shaposhnikova LI, Evchenko Iu M, Levchenko BI, Surkhaev
DB, Korzhov PN, et al. [Hyalomma marginatum Koch in Stavropol' region]. Zh
Mikrobiol Epidemiol Immunobiol. 2001 Nov-Dec(6 Suppl):105-8.
23. Emelianova IN. [Ecology of the tick genus Hyalomma Koch 1844
(Acarina: Ixodidae) in Central Caucasus and adjacent territories].
Stavropol2006.
24. Emelianova IN. Hyalomma Koch, 1844 (ACARI: IXODIDAE) ticks of
Central Precaucasia and surrounding territories. (Distribution, ecology, role
in the natural foci of Crimean-Congo heamorrhagic fever) [MSc]. Stavropol:
State University of Stavropol; 2006.
25. Tokhov Iu M. [Faunistic complex of Ixodidae in Stavropol Region:
Dissemination, epizootic and epidemiologic value, control measures] Stavropol:
Anti-plaque Institute, 2009.
26. Kotti BK, Shaposhnikova LI, Evchenko Iu M, Levchenko BI, Surkhaev
DB, Korzhov PN, et al. [Hyalomma marginatum Koch in Stavropol' region]. Zh
Mikrobiol Epidemiol Immunobiol. 2001 Nov-Dec(6 Suppl):105-8.
27. Romanenko VN. [Visual potentialities of the tick Hyalomma asiaticum
asiaticum (Ixodidae)]. Parazitologiia. 2005 May-Jun;39(3):186-90.
28. Romanenko VN. Ecological bases of ethology of pasture ticks
(Parasitiformes, Ixodidae) in finding and attacking hosts (Экологические основы этологии пастбищных иксодовых клещей
(Parasitiformes, Ixodidae) при поиске и нападении на прокормителей). (In Russian). Bulletin of Tomsk
State University (Вестник Томского государственного университета). 2007 (298):224-8.
29. Apanaskevich DA. [Host-parasite relationships of the genus Hyalomma
Koch, 1844 (Acari, Ixodidae) and their connection with microevolutionary
process]. Parazitologiia. 2004 Nov-Dec;38(6):515-23.
30. Papadopoulos B, Morel PC, Aeschlimann A. Ticks of domestic animals
in the Macedonia region of Greece. Vet Parasitol. 1996 May;63(1-2):25-40.
 |
| Sylvia communis |
 |
| Sylvia communis |
 |
| Sylvia communis |
31. Enigk K, Grittner I. [The rearing and biology of ticks]. Z Parasitenkd. 1953;16(1):56-83.32. Estrada-Pena A,
Martinez Aviles M, Munoz Reoyo MJ. A population model to describe the
distribution and seasonal dynamics of the tick Hyalomma marginatum in the
Mediterranean Basin. Transbound
Emerg Dis. 2011 Jun;58(3):213-23.
33. Hueli
LE. Estudio del ciclo biologico de Hyalomma marginatum marginatum Koch. 1844
(Acarina:Ixodidae) bajo, condiciones estandar de laboratorio. Rev Iber
Parasitol. 1979;39:143-52.
34. Romanenko VN. Ecological bases of ethology of pasture ticks
(Parasitiformes, Ixodidae) in finding and attacking hosts Bull Tomsk State
Univ. 2007:224-8.
35. Estrada-Pena A, Sanchez N, Estrada-Sanchez A. An assessment of the
distribution and spread of the tick Hyalomma marginatum in the western
Palearctic under different climate scenarios. Vector Borne Zoonotic Dis. 2012
Sep;12(9):758-68.
36. Rumer L, Graser E, Hillebrand T, Talaska T, Dautel H, Mediannikov O,
et al. Rickettsia aeschlimannii in Hyalomma marginatum ticks, Germany. Emerg
Infect Dis. 2011 Feb;17(2):325-6.
37. Chochlakis D, Ioannou I, Sandalakis V, Dimitriou T, Kassinis N, Papadopoulos
B, et al. Spotted fever group Rickettsiae in ticks in Cyprus. Microb Ecol. 2012
Feb;63(2):314-23.
38. Tomassone L, Grego E, Auricchio D, Iori A, Giannini F, Rambozzi L.
Lyme borreliosis spirochetes and spotted fever group rickettsiae in ixodid
ticks from Pianosa island, Tuscany Archipelago, Italy. Vector Borne Zoonotic
Dis. 2013 Feb;13(2):84-91.
39. Filipe AR, Casals J. Isolation of Dhori virus from Hyalomma
marginatum ticks in Portugal. Intervirology. 1979;11(2):124-7.
40. Converse JD, Hoogstraal H, Moussa MI, Stek M, Jr., Kaiser MN. Bahig
virus (Tete group) in naturally- and transovarially-infected Hyalomma
marginatum ticks from Egypt and Italy. Arch Gesamte Virusforsch.
1974;46(1-2):29-35.
41. Moussa
MI, Imam IZ, Converse JD, El-Karamany RM. Isolation of Matruh virus from
Hyalomma marginatum ticks in Egypt. J Egypt Public Health Assoc.
1974;49(6):341-8.
42. Turell MJ. Role of ticks in transmission of Crimean-Congo
haemorrhagic fever virus. . In: Ergonul O, Whitehouse CA, editors. Crimean-Congo
hemorrhagic fever: A global perspective. Dordrecht: Springer; 2007.
43. Beeching NJ, Fletcher TE, Hill DR, Thomson GL. Travellers and viral
haemorrhagic fevers: what are the risks? Int J Antimicrob Agents. 2010 Nov;36
Suppl 1:S26-35.
44. Gale P,
Stephenson B, Brouwer A, Martinez M, de la Torre A, Bosch J, et al. Impact of
climate change on risk of incursion of Crimean-Congo haemorrhagic fever virus
in livestock in Europe through migratory birds. J Appl Microbiol. 2012
Feb;112(2):246-57.
45. Horvath LB. Precipitating antibodies to Crimean haemorrhagic fever
virus in human sera collected in Hungary. Acta Microbiol Acad Sci Hung.
1976;23(4):331-5.
46. Filipe AR, Calisher CH, Lazuick J. Antibodies to Congo-Crimean
haemorrhagic fever, Dhori, Thogoto and Bhanja viruses in southern Portugal.
Acta Virol. 1985 Jul;29(4):324-8.
47. Ceianu SC, Raluca P, Daniel C, Lonut C, Aurelia I, Cristian I, et
al., editors. Serological evidence for the circulation of the Crimean-Congo
haemorrhagic fever virus in Romania. Annual meeting ArboZooNet; 2009; St
Raphael, France.
48. Hekimoglu O, Ozer N, Ergunay K, Ozkul A. Species distribution and
detection of Crimean Congo Hemorrhagic Fever Virus (CCHFV) in field-collected
ticks in Ankara Province, Central Anatolia, Turkey. Exp Appl Acarol. 2012
Jan;56(1):75-84.
49. Tekin S, Bursali A, Mutluay N, Keskin A, Dundar E. Crimean-Congo
hemorrhagic fever virus in various ixodid tick species from a highly endemic
area. Vet Parasitol. 2012 May 25;186(3-4):546-52.
50. Yesilbag K, Aydin L, Dincer E, Alpay G, Girisgin AO, Tuncer P, et
al. Tick survey and detection of Crimean-Congo hemorrhagic fever virus in tick
species from a non-endemic area, South Marmara region, Turkey. Exp Appl Acarol.
2013 Jun;60(2):253-61.
51. Gergova I, Kunchev M, Kamarinchev B. Crimean-Congo hemorrhagic fever
virus-tick survey in endemic areas in Bulgaria. J Med Virol. 2012 Apr;84(4):608-14.
52.
Estrada-Pena A, Palomar AM, Santibanez P, Sanchez N, Habela MA, Portillo A, et
al. Crimean-Congo hemorrhagic fever virus in ticks, Southwestern Europe,
2010. Emerg Infect Dis. 2012 Jan;18(1):179-80.
53. Fryauff DJ, Shoukry MA, Schreck CE. Stimulation of attachment in a
camel tick, Hyalomma dromedarii (Acari: Ixodidae): the unintended result of
sublethal exposure to permethrin-impregnated fabric. J Med Entomol. 1994
Jan;31(1):23-9.
54. Fryauff DJ, Shoukry MA, Schreck CE. Stimulation of attachment in a
camel tick, Hyalomma dromedarii (Acari: Ixodidae): the unintended result of
sublethal exposure to permethrin-impregnated fabric. J Med Entomol. 1994
Jan;31(1):23-9.
55. Jameson LJ, Ramadani N, Medlock JM. Possible drivers of
Crimean-Congo hemorrhagic fever virus transmission in Kosova. Vector Borne
Zoonotic Dis. 2012 Sep;12(9):753-7.
56. Fuller RJ, Gough SJ. Changes in sheep numbers in Britain:
implications for bird populations. Biol Conserv. 1999 Nov;91(1):73-89.
57. Smith RK, Jennings NV, Robinson A, Harris S. Conservation of
European hares Lepus europaeus in Britain: is increasing habitat heterogeneity
in farmland the answer? J Appl Ecol. 2004 Dec;41(6):1092-102.
 |
| colirrojo real (Phoenicurus phoenicurus) |
 |
| colirrojo real (Phoenicurus phoenicurus) |
 |
| colirrojo real (Phoenicurus phoenicurus) |
Publicado el 22 de diciembre de 2014 en la web de ecdc European Center for Disease Prevention and Control: http://www.ecdc.europa.eu/en/Pages/home.aspx
Vera artículo original: http://www.ecdc.europa.eu/en/healthtopics/vectors/ticks/Pages/hyalomma-marginatum-.aspx
Todas las imágenes las he obtenido por Google Imágenes tras una búsqueda, por ejemplo, "Hyalomma marginatum". Agradezco a sus autores por compartirlas en la red.


%2Bmarginatum%2BRufipes%2BKoch%2Bmapa.jpg)

No hay comentarios:
Publicar un comentario